1. はじめに
近年、水素の抗酸化物質としての可能性について、多くの研究が進んできました。現在では、抗酸化物質であるという特徴のほか、エネルギー代謝への作用、また、一番小さな分子ゆえの透過性という優位な点を活かした脳や各細胞への作用など、その可能性と期待は高まってきています。医学的側面以外でも、一般市場においては、エイジングケア、インナービューティー及び運動効果という視点で注目度を増してきています。
一方、水素は、固定化に技術が必要とされるため、結果として水素商品の評価においても、専用の機器を有する等、製造者側の判断基準に従うしかないといった側面も拭いきれません。現在でも、水素そのものの存在の証明において、業界に統一した指標がないなど、可能性の一方で、不明瞭さも指摘されております。
このような背景から、ここでは、水素の効果についての詳しい考察はほかに譲り、市場に導入する際の水素商品の基準をどこに置くか、エビデンスを元にした開発基準をご紹介させていただけたらと考えております。
2. 効果と安全性についての考察
1) 水素の測定方法と数値化
水素の価値をどこに置くかという観点から、その評価指標も変わってきます。水素量と言った際に、水素濃度が大切であるという研究のほか、効果に重きをおく研究もあります。ただ、それぞれに共通しているのは、不安定な水素をいかに留めておくかという視点に立って、研究開発されているということです。目的は同じで、アプローチの仕方が異なるということです。
当社が採用している、水素吸着素材(以下 HCP)は、水素ガス(水素分子)を正確に測定できる「ガスクロマトグラフ (以下GC)」での数値化が基準となっています。この機器の特徴は、水素ガス(水素分子)以外の要素を排除して、水素ガス(水素分子)のみを直接、正確に測定できる点です。一方、水素には、還元作用がありますので、酸化還元電位計や溶存水素計という還元力を一つの指標として数値化することもあります。こちらは、液体に含まれる水素量を測定するのに優れていると考えられていますが、水素以外の還元物質に反応して数値化されることがあるので、正確な水素量という面では、GCが一番優れています。
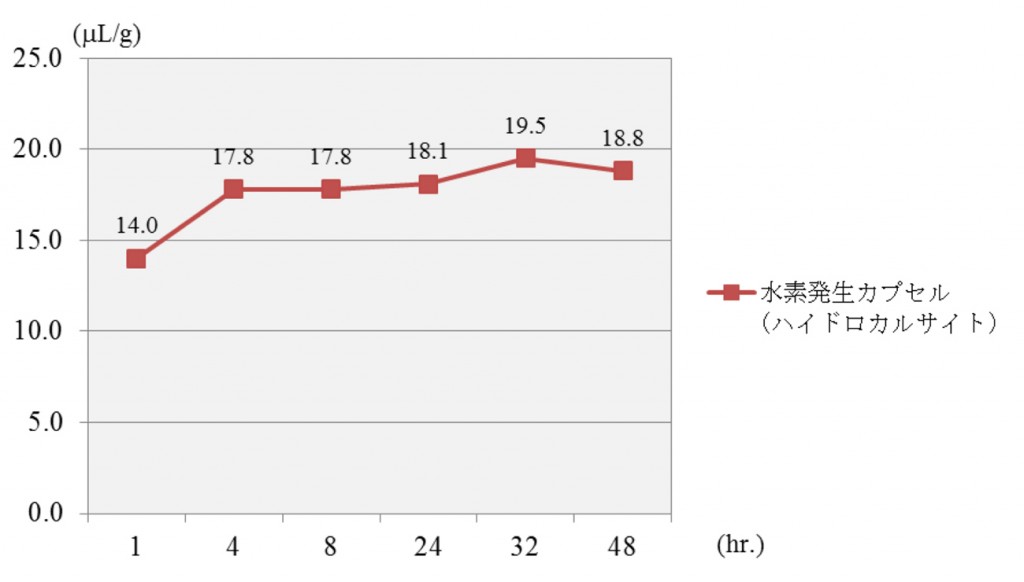
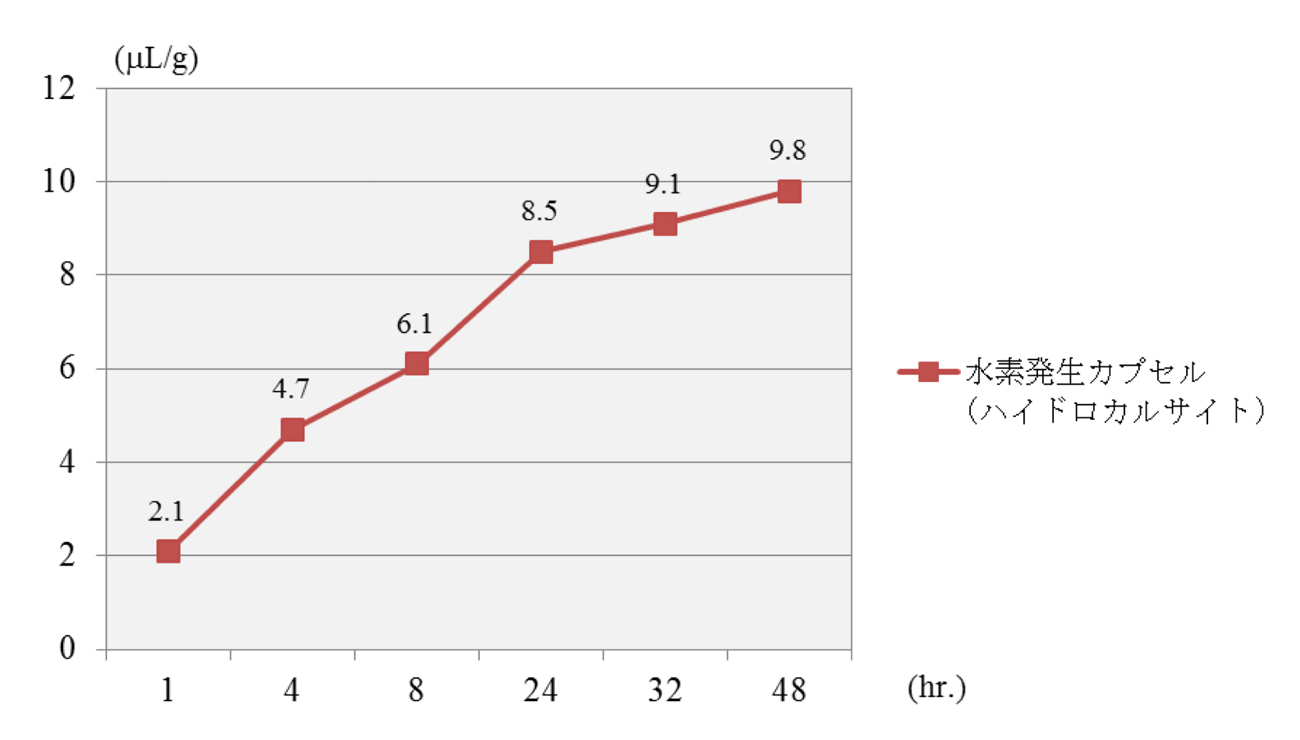
図1に示すのが、当社で採用しているHCPから発生する水素量をGCにて評価した結果です。
図1:H2発生量(µL/g)と経過時間
(素材:2014年4月製造品、第三者機関にて実施)
水素発生量は、密閉容器に粉末と水を入れ、気相部に発生した水素ガス(水素分子)を測定しました。粉末が純水に触れ始めてから水素ガス(水素分子)は徐々に発生し、ほぼ4時間後に平衡状態に達していることが確認できます。このように含有量を数値化することで、水素に関する様々な研究発表データとリンケージさせることが可能となります。
水素の固定化には、製造特許(特許第4472022)を元に加工されています。HCPと比較し、サンゴカルシウムを含む他の多孔質素材で加工した際の水素発生量を表1に示しております。こちらのデータはラボで加工した際のデータとなります。(ちなみに、図1は、ラボでの成果を反映し、生産ラインに乗せて加工した際に得られたデータとなります)
表1:同様の他素材含む水素データ(特許第4472022より抽出)
GCによる水素の定量分析(第三者機関にて実施)
| 水素ガス含有量(µL/g) | ||||||
|---|---|---|---|---|---|---|
| 経過時間(時間) | ||||||
| 1 | 4 | 8 | 24 | 32 | 48 | |
| 実施例 1 | 14.5 | 20.8 | 23.6 | 28.5 | 29.5 | 29.9 |
| 比較例 1 | 0.02 | 0.05 | 0.06 | 0.04 | 0.04 | 0.05 |
| 比較例 2 | 0.04 | 0.05 | 0.06 | 0.07 | 0.07 | 0.09 |
| 比較例 3 | 0 | 0.02 | 0.06 | 0.14 | 0.18 | 0.23 |
| 比較例 4 | 0.04 | 0.04 | 0.04 | 0.02 | 0.02 | 0.02 |
| 比較例 5 | 0 | 0 | 0 | 0.01 | 0.01 | 0.01 |
実施例1:HCP
比較例1:重質炭酸カルシウム
比較例2:卵殻炭酸カルシウム
比較例3:珊瑚由来の重質炭酸カルシウム
比較例4:ゼオライト粉
比較例5:沈降炭酸カルシウム
その結果、HCPにおいては、同じ多孔質を有する素材であっても、その他のものと比較し、明らかに水素が吸着していることが確認されました。
水素のキャリア-である液体と粉末 (固体) という異なる組成のものを横並びにして比較することは、厳密には困難ですが、ほぼ1mL=1gと単位を絞ることで、検証することができます。一般的に液体で示される飽和水素濃度は、1.6ppmと言われています。図1のGCで示された水素量(1gあたりどれだけの水素量が含まれているか)をppmという濃度に換算すると以下のようになります。気体の体積1molは22.4L(水素2g)であり、水素発生カプセルの水素量19.5µL/g をグラム単位に換算すると、
2(g):22.4(L)=X(g):19.5×10-6(L)
X=1.7×10-6(g)=1.7µg
よって、水素発生カプセル1gあたりは、1.7µgの水素が含まれ、すなわち1.7ppmといえる。
濃度という側面だけで比較すると、粉末1gあたりで、飽和水素水1.6ppm相当とほぼ同等の数値ということになります。あとは、摂取量や摂取方法、摂取環境などの違いを加味しながら、水素の吸収を示唆する必要があります。
また、数値化することで効果に関する仮説も立てやすくなります。例えば、九州大学の水素研究(抗酸化物質としての水素分子:“水素医学”の期待と展望)において、濃度に関して1.6ppmも0.08ppmを効果が変わらないという報告があります。つまり、量の側面を加味せず、濃度を中心として検証した場合、この0.08ppmが効果を示す最小有効単位であるとすれば、上記粉末の水素量で換算すると、1gで1.7ppmですから、約50mg摂取で0.08ppm相当ということになります。
もちろん、実際には、摂取される方の身体の大きさや疲労度・疾病の度合いなどによって、体感値は、異なると思われますが、数値化されていることで配合量の背景も論じることができます。少なくとも、適切な摂取目安に対する質問などに対して、水素は、今のところ副作用が見当たらないので、どれだけ取っても大丈夫というような場当たり的で、不明瞭な回答をしなくて済みます。
2) 摂取環境下での水素発生量
水素は、拡散性が高く、抜けやすいのが課題です。効率的に人体にどれだけ摂り込まれているか見積もれる材料が必要です。商品に高濃度の水素が入っていますと主張しても、摂取時の環境が重要であり、ユーザーが実際に使用する環境はそれぞれですから、必ずしも製造者が推奨する環境ばかりとは限りません。以下は、体内環境を想定した、水素発生量をGCにて測定したデータになります (図2)。
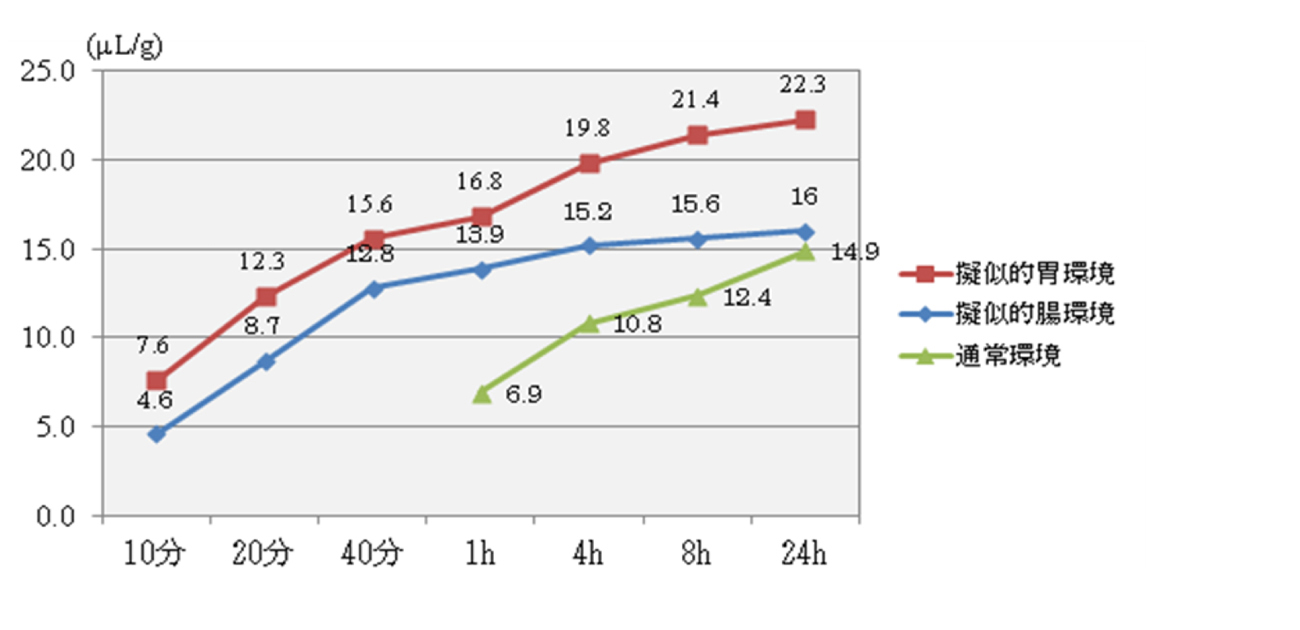
図2:擬似的消化管環境下でのH2発生量(µL/g)と経過時間
(測定:2012年11月、第三者機関にて実施)
試料及び機器:塩酸-塩化カリウム緩衝液(pH=1.2)、リン酸緩衝液(PBS, pH=6.8)、純水、ガスクロマトグラフ(島津GC-14AT)、データ処理装置(島津クロマトパックC-R7A)
その結果、体内環境においても、HCPから水素が発生することが推察されます。また、同じ素材でも、酸性寄り(擬似的胃液)に分解が進むことで、通常の分析データから得られる数値より多くの水素ガス(水素分子)を発生することが示唆されました。
なお、通常環境(純水)での分析について、純水のpHは想定済で素材の分解がそれほど速く進まず、急速に水素が発生するとは考え難いため、1h経過後から分析を開始しました。
表2:素材のpH測定
| 測定結果 | 胃環境 | 腸環境 | 純水 | |||
|---|---|---|---|---|---|---|
| 採取量(g) | pH | 採取量(g) | pH | 採取量(g) | pH | |
| 水素カプセル(HCP400mg配合) | 2.9997 | 6.24 | 3.0273 | 7.02 | 2.9922 | 9.72 |
使用機器: Horiba F-55 pH meter
初期緩衝液:擬似的胃環境(HCl/KCl, pH= 1.257)、擬似的腸環境(PBS, pH= 6.821)
その結果、HCPは、純水環境で弱アルカリを示していたものが、擬似的な胃環境(強酸性)及び腸環境(中性)に向かうと、中性寄りの数値が導き出されました。この推移は、原料の主成分(炭酸カルシウム)による中和的反応の結果であると考えることができます。
本来であれば、腸液では更に中性~酸性寄りであるとみられますが、今回実験で使用した擬似的な液体はごく微量ゆえ、かつ擬似的な胃液よりも腸液の方がpH変動がし難い。実際、生体内に入って通常の食品としてのプロセスを踏めば、胃を通過後、各消化液によって弱酸性に依存し、かつ実験よりも多くの消化液に浸されることが推察されます。
*参考:一般的な食物の流れ
① pH
口腔(pH=7) ⇒ 食道(pH=7) ⇒ 胃(食前食後pH=1~2、食中pH=3~4)
⇒ 十二指腸(pH=6~7) ⇒ 小腸(pH=5~6) ⇒ 大腸(pH=5~7)
② 時間
口腔~食道(固体物30~60秒) ⇒ 胃(滞在時間約4h、胃液で一部を吸収)
⇒ 小腸(十二指腸・空腸・回腸、滞在時間約7~9h、栄養分・水分を消化吸収)
⇒ 大腸(結腸・直腸、滞在時間約25~30h、食物のカスや腸内細菌などが混ざり便となる)
結論として、摂取環境下での水素発生量とpH値から鑑みると、実際には、カプセルや錠剤等の性質によって、どこで素材が水分に触れ、水素ガス(水素分子)の発生及び吸収がなされるのか厳密には測れませんが、本検討結果から、水素ガス(水素分子)の発生と吸収を示唆することは十分可能であると考察できます。
3) トレースのとれる素材
粉末の水素素材の場合、水素を留めておくスペースが必要になりますので、多孔質な素材が採用されるケースが多いです。中でも、サンゴカルシウムは、汎用される素材です。
サンゴは、自然保護の観点からワシントン条約によって制限されていますので、採取においては、日本でも、砂利採取法に基づいた許認可制で、死滅したものを採取し、食品に応用する際は、既存添加物という扱いで流通されています。天然のものは、有機物も多く含み、これを付加価値として捉え、販売されているメーカーも散見されます。
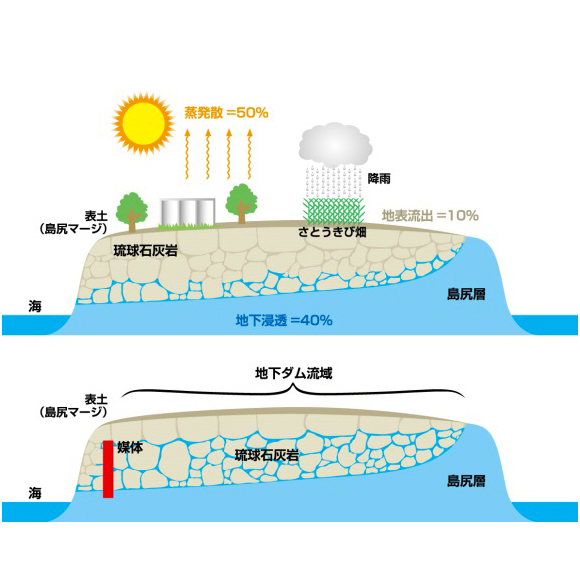
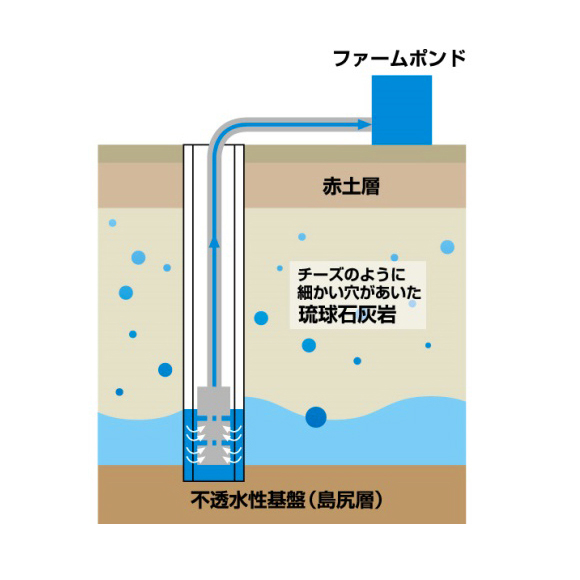
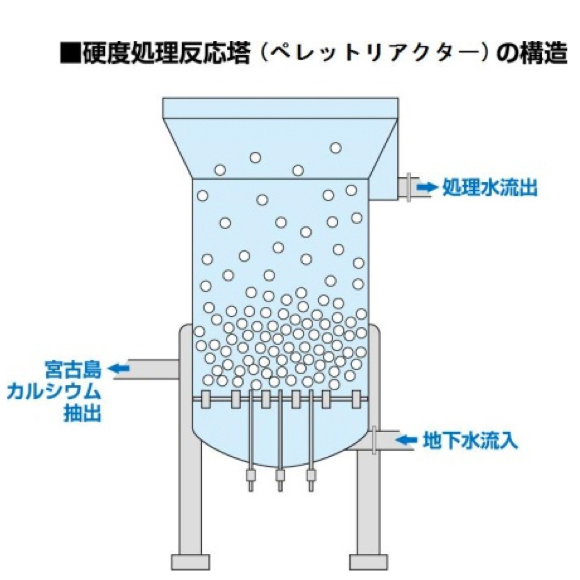
一方、当社で採用している素材は、同じサンゴ系でも採取方法が異なり、沖縄県宮古島市において、この土地ならではの特徴を活かした独特な方法で得られるカルシウムを採用しています。宮古島自体は、琉球石灰岩(サンゴ礁)が隆起してできた島であり、世界で最も若い石灰岩に覆われています。沖縄本島周辺の石灰岩層とも異なる、この地域独自の石灰岩層です。その下には水を通しにくい島尻層が広がっている為、地下水は、下に漏れることなく、石灰岩の小さな穴や隙間に留まります。石灰岩が天然のろ過装置にもなっています。普通であれば、低い方の海に流れ出てしまいますが、そこを堰き止めることで石灰岩に地下水が留まります(図3a)。宮古島には、川がありませんので、この地下水を汲み上げることで大事な生活水となります(図3b)。しかしながら、宮古島の石灰岩層は、世界で最も若い石灰岩層ゆえに溶け出しやすく、類まれな硬水であり、そのままでは生活水として使用できません。そこで、晶析法という硬水を軟水化させる工程を踏み (図3c)、硬水に含まれるカルシウム成分を除去します。この工程は、行政によって行われています。
図3:宮古島における給水システム
a. サンゴ礁が隆起してできた島・宮古島
b. 地下ダムからの汲み上げ(市の水道局)
c. 硬度軟水化施設
一般的に水素素材として採用される素材は、天然のものが多く、有機物も豊富ですが、それゆえ、組成がロットごとに異なりやすいという宿命にあります。水素を安定的に吸着させる上で、素材の組成が均一であるということは重要です。
上記の宮古島での方法によると、ほぼ毎回均一な素材が出来上がります。水素を吸着させる上で、また、同じクオリティの製品を維持するという意味でも大切な要素が備わっていると言えます。また、このように抽出方法の異なる方法で得られた素材は、一般的なサンゴカルシウムと結晶構造のほか、ミネラル数にも明らかな違いが生まれました。


図4:結晶構造解析
a. サンゴカルシウム
b. 宮古島産カルシウム
撮影:株式会社セイシン企業 古河開発研究所 粉体測定センター
使用機器:JSM5410(日本電子製)
図4aに示された一般的なサンゴカルシウムの結晶構造は、アラゴナイトと呼ばれます。一方、晶析法によって抽出された宮古島産カルシウム(図4b)の結晶構造は、カルサイトと呼ばれます。一般に、カルサイトの方が溶けにくく、吸収し難いと言われています。一方で、アラゴナイト型は、吸収性を付加価値として、捉える事ができます。基材に何を求めるかによって、優位点が異なります。
微量元素(ミネラル)の含有量を調べた結果、弊社で採用しているHCPにおいては、他のサンゴ系素材に比べ、非常に少ないミネラル数であると考えられ、比較的合成品に近いデータが導き出されました (表3)。工業的に作られた素材ゆえの結果であると考えられます。
表3:宮古島カルシウムのミネラルデータ(日本食品分析センター調べ, 単位は100gあたり)
| ミネラル名 | 分析結果 | ミネラル名 | 分析結果 |
|---|---|---|---|
| Ca (カルシウム) | 39.4g | Fe (鉄) | 3.62mg |
| Mg (マグネシウム) | 283mg | P (リン) | 10.2mg |
| Na (ナトリウム) | 67.5mg | S (イオウ) | 0.03g |
宮古島カルシウムと同様の主成分をもつ、サンゴを含む幾つかの素材を集めて、微量元素(ミネラル)の定性分析を行ったところ、海洋由来のものは、総じてストロンチウム量が高く、他のものと分類できることが示唆されました。また、化学合成品については、マグネシウムの存在がほとんど認められませんでした。これらストロンチウム含量とマグネシウム含量に着目した場合、HCPにおいては、ストロンチウム含量が海洋由来のものよりも低く、合成品よりもマグネシウム含量が高い結果となり、一般的なサンゴカルシウムと区分が異なることが示唆されました (データ不記載)。
ゆえに、非常に独特な多孔質性を有した、オリジナリティのある素材ということが言えます。保健所および管轄関連機関の指導の元、HCPは、食品分類のカルシウムという扱いとなりますが、抽出方法やこれらデータから判断しても、その区分が妥当であると考えられます。
3. 水素分子の課題への対応
1) 特許技術
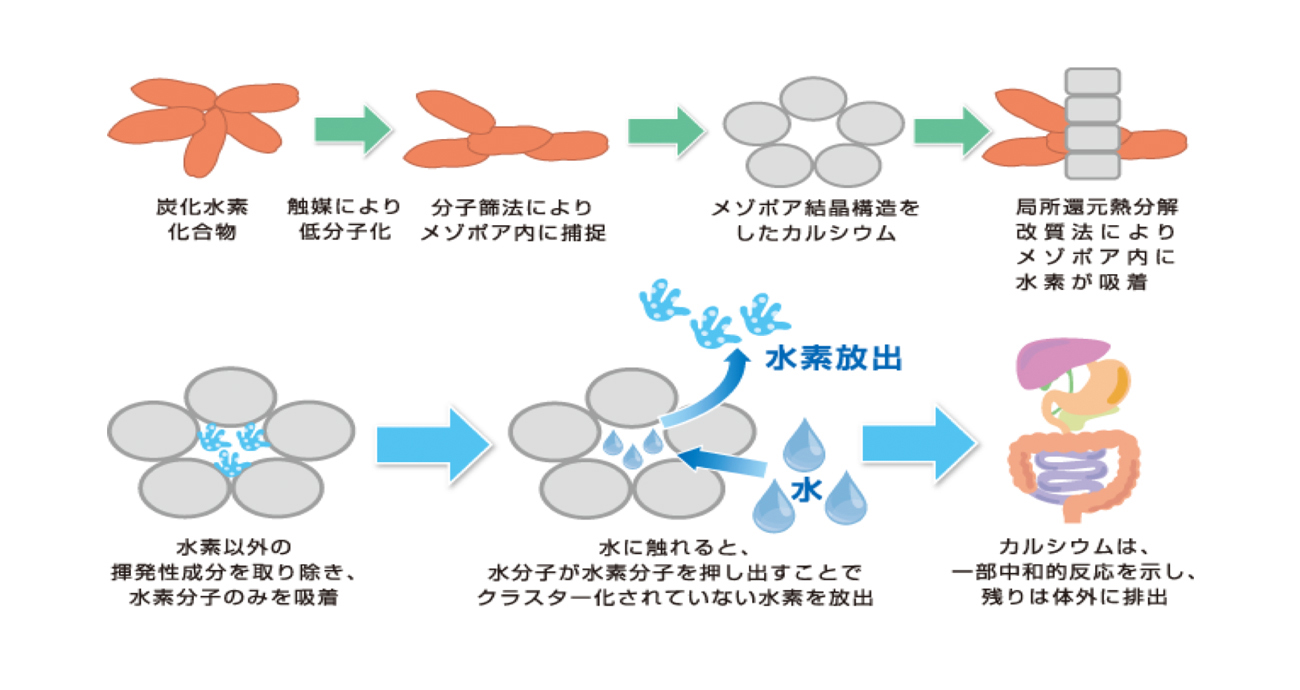
組成が安定した素材の採用の次は、水素吸着工程へと移ります。HCPは、製造特許(特許第4472022)を元に作られています。特許内容は、細かくなりますが、工程そのものを大枠で捉えると、食品の殺菌洗浄工程の応用の中で、水素吸着反応が見られるということになります(図5)。何か特別な手を加えたり、組成を変化させたりというよりは、素材そのものを活かし、環境や自然にも優しい方法で加工されています。
図5:水素吸着メカニズム
この工程では、カルシウムを炭化水素系溶液に浸し、乾燥に近い温度で熱処理します。この時、細孔内は、細孔外部から酸素が供給されにくくなり、低酸素雰囲気状態となり乾留状態で熱分解され、溶液が低分子化されます。つまり、溶液は、細孔内で低分子化され、最後に水素ガス(水素分子)が残り、細孔内に物理的に含有されると考えられます。低温での焼成のため、主成分や結晶構造に変化はなく、原料そのものは、白色のままであり、副生成物の発生もみられません。安定的に水素吸着がなされます。
均一な素材組成と特許製法により、吸着される水素量は毎回ほぼ同じ量であることをGCにて確認しています。本来、不安定な水素の発生をきちんと確認できるということだけでなく、ある程度、毎回水素量をコントロールできるということは、特筆すべき点であると考えられます。
また、これらが小スケールではなく、量産体制で製造する際に再現できなければ、意味がありません。通常、水素加工における熱処理は、一度に大量の素材を入れた大きな炉で行われます。その結果、抽出箇所によって、水素吸着がまばらになることが考えられますが、HCPにおいては、他にはないオリジナルに製造された炉によって、少量ずつ均等に同じ時間、同じ温度の熱が加わるよう加工されています (図6)。非常に時間と手間のかかる職人作業となりますが、これにより何処を抽出してもほぼ同じ水素量の素材が出来上がります。しかも、低温での熱処理になりますので、高温処理する同様他素材に比べても副生成物発生の可能性は、限りなく少なくなります。


図6:専用炉による熱処理加工
2) 水素の経時変化率
水素の課題は、透過しやすく、気散しやすいという点です。技術が進歩し、液体もしくは固体に水素を、溶存あるいは吸着させることができたとしても、製造時だけでは、意味がありません。水素を扱う上では、保存環境や摂取環境によっても左右されるということが考慮されなければなりません。
そこで、通常環境で保管した同素材の水素含有量の経時変化をGCによって、測定しました (図7)。
図7:水素の経時変化測定(製造から2年半経過後・通常環境にて保管)
分析素材:製造ロット番号10P0519A0728H0808 第三者機関にて実施
宮古島カルシウムに水素を吸着させた場合、平均して約15µL/g以上の水素量が確認できますが、賞味期限の間(約3年)で、年間約10%の減少率に押さえられていることから、経時変化の少ない素材であると言えます。
特に水素は、目に見えない不安定なものなので、言ったもの勝ちということではなく、一般的に受け入れ可能な情報を揃える必要があります。その為にも素材選定、加工方法、品質証明、品質保持において見積もれるデータの取得が肝要です。
4. まとめ
1) 水素ガス(水素分子)発生の安定性が意味するところ
水素の効果に関する研究が進み、その可能性に期待が高まる一方で、水素は、まだまだわからないことが多いのも事実です。その中で、できる限り水素量を管理し、最大限、人体にどれくらい摂り込まれているか推定することができた上で商品化し、体感をいただいています。水素量の測定においても、我々は、水素だけを直接測定した数値をお示ししているので、他の報告事例とリンケージさせることもできます。今後もこのように効果に対する仮説を立てやすい材料を揃えて、商品化に役立てていきたいと考えています。